Решебник химии восьмого класса к учебнику Г.Е.Рудзитиса и Ф.Г. Фельдмана
Сборник подробных ответов с пояснениями составлен на базе учебника химии Рудзитиса 2016 года. Учебник рекомендован Министерством образования и науки Российской Федерации для общеобразовательных организаций. Все параграфы решебника идентичны книге. В готовые домашние задания включены не только упражнения, но и тесты, практические работы, лабораторные опыты.
Учебник содержит 8 глав и 57 параграфов. Между новыми темами размещены практические работы. Материал начинается с введения в предмет и базовых понятий химии, включает как теорию, так и задачи.
Учебное пособие от Ответкина поможет в изучении тем по химии 8 класса, таких как:
- Химия и ее базовые понятия, методы познания.
- Вещества: чистые, молекулярного и немолекулярного строения, простые и сложные. Свойства веществ. Закон постоянства состава веществ. Закон сохранения массы веществ.
- Физические и химические явления.
- Молекулы, ионы, атомы.
- Атомно-молекулярное строение.
- Валентность.
- Относительная молекулярная масса.
- Химические элементы и их знаки.
- Химические формулы и работа с ними.
- Химические реакции и их типы.
- Кислород, его свойства, нахождение в природе, получение и применение.
- Озон. Состав воздуха.
- Характеристики водорода, его свойства, нахождение в природе, получение и применение.
- Свойства воды, способы ее применения.
- Растворы.
- Количество вещества и молярная масса. Моль.
- Молярный объем газов. Закон Авогардо.
- Оксиды. Гидроксиды. Кислоты. Соли. Их химические свойства.
- Классификация химических элементов. Таблица Менделеева.
- Периодический закон Менделеева и его значение.
- Электроотрицательность химических элементов.
- Степень окисления.
Достоинства решебника по химии за 9 класс учебник Рудзитис
Портал станет надежным помощником и незаменимым союзником для каждого ученика, желающего добиться высоких результатов по такой непростой, но интересной дисциплине. Решебник поможет подростку нейтрализовать имеющиеся трудности в учебном процессе и сократить отставание от школьной программы. Он гарантирует правильность выполнения домашнего задания, ведь содержит в себе исключительно верные ответы и подробные пояснения авторов к решению каждого упражнения из дидактического материала. Благодаря этому ученик сможет не только подтянуть имеющиеся оценки и улучшить свою успеваемость, но и обрести множество новых знаний. Рассмотрим другие плюсы учебно-методического комплекса ГДЗ:
- Размещено в онлайн-формате и доступно к использованию круглосуточно.
- Даст возможность обрести уверенность в себе и перестать бояться получить двойку за некачественную подготовку к уроку.
- Простой и понятный интерфейс поиска верных ответов по номеру упражнения из учебника.
- Позволит закрепить пройденный в школе материал.
К тому же, если школьник научится правильно использовать вспомогательный ресурс в учёбе, то сможет существенно сократить среднее время подготовки к урокам. Электронным сборником могут воспользоваться как школьники, серьезно отстающие от программы, так и отличники. Если в первом случае справочное пособие поможет повысить академическую успеваемость, то во втором — ребята смогут совершать самопроверку регулярно и устранять самостоятельно систематические ошибки. Задача родителей — оказать своевременную моральную поддержку. Цель решебника — помочь ему в трудную минуту.
Каким образом помогут ГДЗ по химии для 9 класса (авторы: Г. Е. Рудзитис, Ф. Г. Фельдман)
Отличники и многие хорошисты обычно имеют явное преимущество перед своими сверстниками:
- Они иногда могут пропускать занятия. Происходит это из-за того, что они – любимчики учителей. Их целеустремленность, пунктуальность и умение сосредотачиваться подкупают и служат гарантом, что ни одна тема не будет упущена, а все заданные упражнения будут выполнены;
- Бонусы при поступлении приносит посещение конкурсов и олимпиад. Помимо этого, такая активность позволяет меньше волноваться на контрольных работах, тестах, ЕГЭ и ОГЭ;
- Они почти никогда не подвергаются травле со стороны одноклассников.
Чтобы добиться такого положения, необходимо стараться. Так, требуется не прогуливать учебу без повода, заниматься дополнительно и выявлять все пробелы и упущенные моменты. Особенно это касается науки о веществах. Она нужна для значительного спектра специальностей, но все же большинство не выбирают эту дисциплину в качестве государственного экзамена, однако получить заветную медаль мечтает каждый.
Как пользоваться сайтом и открывать ответы с комментариями?
Это можно сделать через социальные сети:
После этого автоматически будет создан аккаунт с личным кабинетом. Пользователь получает доступ к подробным решениям.
Также можно зарегистрироваться с нуля с помощью электронной почты:
С завершением регистрации пользователь получает доступ в свой личный кабинет и может открывать подробные комментарии к заданиям.
В личном кабинете есть три главные вкладки: «Ваш профиль», «Подписка», «Подробные решения».
В профиле вбит логин и электронный адрес, там можно изменить пароль, подписаться на рассылку с сайта.
Подписка по умолчанию бесплатная, дает доступ к трем подробным ответам в сутки. Если этого недостаточно, можно получить большее количество открываний в день, приобретя платную подписку по символическим расценкам.
Во вкладке «Подробные решения» видны все просмотренные решебники и упражнения, они сохраняются в личном кабинете в течение 24 часов. Их можно открывать неограниченное количество раз, быстро переходить от одного номера к другому.
Химические свойства
1. Сульфат натрия может реагировать с простыми веществами :
1.1. Сульфат натрия реагирует со фтором при температуре 100–150º C. При этом образуются фторид натрия, сульфурилфторид и кислород:
1.2. С водородом сульфат натрия реагирует при температуре 550–600º C, в присутствии катализатора Fe2O3 с образованием сульфида натрия и воды:
2. Сульфат натрия вступает в реакцию со многими сложными веществами :
2.1. Сульфат натрия реагирует с гидроксидом бария с образованием гидроксида натрия и сульфата бария:
2.2. При взаимодействии с концентрированной серной кислотой твердый сульфат натрия образует гидросульфат натрия:
2.3. Сульфат натрия реагирует с оксидом серы (VI) . Взаимодействие сульфата натрия с оксидом серы (VI) приводит к образованию пиросульфата натрия:
2.4. Сульфат натрия взаимодействует с хлоридом бария . При этом образуются хлорид натрия и сульфат бария:
http://gomolog.ru/reshebniki/8-klass/gabrielyan-2013/prakt/6.html
http://gdzwow.com/answers/9-himiya-uch-rudzitis-vopr-k-par-22.html
Готовые домашние задания для 8 класса по химии Рудзитиса
Если раньше к решебникам относились скептически, то сегодня времена изменились. С появлением нового формата ГДЗ школьники не просто переписывают короткие решения в тетрадь, но и восполняют пробелы в знаниях, занимаются самопроверкой, готовятся к контрольным работам.
Ответкин предоставляет уникальный учебный материал, который является важным дополнением к школьной программе. С помощью наших подробных ответов с комментариями ученики понимают алгоритм выполнения задач, проясняют для себя ключевые моменты в новой сложной теме.
Почему Ответкин пользуется популярностью у школьников и их родителей?
- Авторские подробные комментарии. На нашем сайте собран качественный материал, который разрабатывали лучшие учителя России. К большинству ответов есть подробные пояснения, которые в подавляющих случаях понятнее, чем теория из учебника. Видя правильный механизм решения того или иного упражнения, школьник понимает суть метода, учится выполнять аналогичные задания.
- Круглосуточный доступ. Ответкин приходит на помощь в любое время суток и в любой ситуации: когда нужно быстро исправить плохую оценку, подсмотреть ответ во время самостоятельной, проверить себя при выполнении домашней работы. Зайти на сайт можно с любого устройства, в том числе и мобильного телефона.
- Актуальные данные. Все разделы нашего онлайн-пособия идентичны параграфам учебника, поэтому у школьника не займет много времени поиск нужного номера. Мы размещаем готовые домашние задания только по актуальным учебникам, которыми сейчас пользуются в большинстве школ РФ. Кроме того, формат ответов соответствует всем требованиям ФГОС.
- Экономия денег. Ответкин помогает быстро повысить успеваемость на бесплатной основе, ведь далеко не все дети могут ходить к репетиторам за деньги. Благодаря нашему сайту у каждого школьника есть возможность понять предмет, а не просто бездумно списать готовое решение.
Мы учли, что больше 80% пользователей посещают Ответкин с мобильных телефонов. Поэтому наши материалы размещены в удобном для смартфона формате, с вертикальным расположением текста. Поисковая строка в шапке сайта позволяет найти нужный номер задания в считанные секунды. Достаточно лишь ввести название учебника и его автора.
§ 22. Практическая работа №4
1. Даны пробирки с растворами: а) сульфата натрия; б) хлорида натрия; в) серной кислоты. Опытным путём определите, в какой пробирке находится каждое из указанных веществ.
Поместили лакмус и нитрат серебра в три пробирки с растворами
В пробирке, где находилась серная кислота, лакмус окрасился в красный цвет. в пробирке. где находился хлорид натрия, после добавления нитрата серебра выпал белый осадок.
Серная кислота при взаимодействии с лакмусом окрашивает его в красный цвет (кислота закисляет среду, остальные две соли образованы сильными основаниями и сильными кислотами→не гидролизируются и дают нейтральную среду→лакмус не меняет цвет.)
Качественная реакция на хлориды — выпадение белого осадка хлорида серебра:
В пробирке. где лакмус не поменял цвет. находится сульфат натрия.
2. Дан раствор сульфата меди (II). Получите из него раствор хлорида меди(II).
Поместили к раствору сульфата меди раствор хлорида бария.
Сульфат бария выпадает в осадок.
Качественной реакцией а сульфаты является выпадение осадка сульфата бария. Одновременно таким способом можно получить и хлорид меди:
Добавили к сульфиду калия сульфат меди, к сульфату калия добавили хлорид бария, к сульфиту калия – соляную кислоту, к бромату калия – нитрат серебра.
В пробирке с сульфидом калия выпал черный осадок, с сульфатом калия – белый осадок, с бромидом калия – желтый осадок, с сульфитом калия – появился резкий запах.
С помощью качественных реакции можно определить каждый представленный анион:
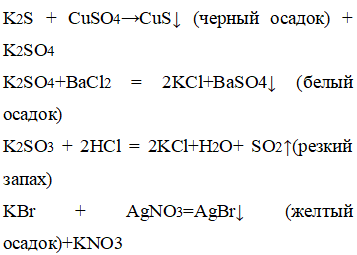
а) цинк→сульфат цинка→гидроксид цинка
б) оксид меди(II)→сульфат меди(II)→гидроксид меди(II)
а) К цинку добавили серную кислоту, а далее гидроксид натрия.
б) К оксиду меди добавили серную кислоту, а далее гидроксид натрия.
а) Вследствие добавления кислоты образовались пузырьки газа, вследствие добавления щелочи образовался белый осадок.
б) Вследствие добавления кислоты образовался синий раствор, вследствие добавления щелочи образовался синий осадок.
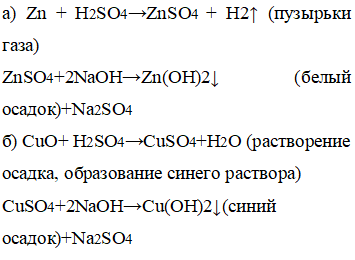
Добавили к цинку, нитрату стронция, хлориду натрия, хлориду кальция и хлориду меди серную кислоту.
При взаимодействии серной кислоты с цинком образовались пузырьки газа (окислитель-восстановительная реакция — цинк и водород изменяют свои степени окисления), с нитратом стронция — выпал белый осадок, с хлоридами натрия и меди — реакции нет.
Реакция с серной кислотой идёт с металлами, стоящими в электрохимическом ряду до водорода, с солями, если в результате реакции выпадает осадок и вытесняет летучие кислоты из солей.
6. Проделайте реакции, подтверждающие качественный состав серной и соляной кислот.
Добавили к соляной и серной кислоте лакмус; поместили к соляной кислоте нитрат серебра, к серной кислоте добавили хлорид бария.
Лакмус окрасился в красный цвет; после добавления реагентов выпали белые осадки. Тот факт, что лакмус окрасился в красный, говорит о том, что в составе веществ присутствует H+.
Появление осадка хлорида серебра говорит о наличии в составе соляной кислоты хлорид-аниона:
Появление осадка сульфата бария говорит о наличии в составе серной кислоты сульфат-аниона:
Ответы из решебника — надежная помощь
Хоть на уроках учителя и стараются всячески донести до своих подопечных все тематические нюансы, но по факту нужная информация откладывается в памяти очень небольшого процента ребят. Остальные же, садясь за выполнение д/з, впадают в ступор, так как не понимают, каким образом им действовать дальше. В сборнике ответов по химии 9 класс Рудзитиса ученики почерпнут все недостающие сведения и пояснения.
Авторы пособия разместили в нем:
- верные ответы для быстрой сверки результатов;
- готовые решения, чтобы можно было понять, откуда взялись недочеты;
- наглядные примеры, чтобы осознать, что требуется делать;
- дополнительные примечания для разбора проблемных параграфов.
С решебником учебный процесс станет более продуктивным, так как подростки смогут своевременно устранять пробелы и пополнять свои навыки. Но им стоит понимать, что обычным списыванием этого не добиться. Справочник стоит использовать только для самоконтроля и работы над ошибками.
Польза решебника по химии за 9 класс учебник Рудзитис Г. Е., Фельдман Ф. Г. (Просвещение)
Чтобы выучить химию, школьникам необходимо усердно работать и, конечно же, использовать справочное пособие в виде ГДЗ. Родителям не стоит переживать за достоверность информации в книге, так как, во-первых, она была неоднократно проверена. Во-вторых, решебник соответствует всем строгим требованиям ФГОС. Отметим, что химия является одним из сложнейших предметов школьной программы для средних и старших классов, так как содержит в себе множество научных терминов и понятий. Поэтому ребятам стоит внимательно отнестись к изучению следующих параграфов из учебника:
- состав атомных ядер;
- ковалентная полярная связь;
- закономерности изменения электроотрицательности элементов в группе и периоде.
Специально подобранный учебно-методический комплекс поможет ученикам в кратчайшие сроки освоить представленные выше разделы учебника и получить положительную оценку в итоговый аттестат. Пособие ГДЗ отлично подойдет и взрослым. Мамы и папы, использующие решебник, смогут не только контролировать процесс самостоятельной подготовки ребенка к занятиям, но и его успехи в работе на уроке. У родителей появится отличная возможность сверить результаты школьника с верными ответами из ГДЗ и помочь ему разобрать непонятные моменты и допущенные ошибки.
Ответы на задания по химии за девятый класс к учебнику Рудзитис Г.Е., Фельдман Ф.Г.
Глава I
Лабораторные опыты:
задание-1задание-2задание-3задание-4
Практические работы:
задача-1задача-2задача-3задача-4задача-5задача-6
§§1-3 :
вопрос-1задача-1задача-2вопрос-2вопрос-3вопрос-4вопрос-5вопрос-6вопрос-7вопрос-8вопрос-9вопрос-10
§§4-6 :
вопрос-1задача-1вопрос-2задача-2вопрос-3задача-3вопрос-4вопрос-5вопрос-6вопрос-7вопрос-8вопрос-9вопрос-10
Глава VII
Лабораторные опыты:
Практические работы:
§ 43-44:
Вопрос 1Задача 1Вопрос 2Задача 2Вопрос 3Задача 3Задача 4Вопрос 4Вопрос 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10
Глава II
Лабораторные работы:
Практические работы:
Задача 1Задача 2Задача 3Задача 4Задача 5Задача 6
§13:
Задача 1Вопрос 1Вопрос 2Задача 2Вопрос 3Вопрос 4
§14:
Вопрос 1Вопрос 2Вопрос 3Вопрос 4Вопрос 5
§§7-10:
Задача 1Вопрос 1Вопрос 2Задача 2Вопрос 3Вопрос 4Вопрос 5Вопрос 6
§11-12:
Вопрос 1Задача 1Задача 2Вопрос 2Вопрос 3Вопрос 4Вопрос 5
Глава VI
Лабораторная работа:
Практические работы:
§ 39:
Вопрос 1Задача 1Вопрос 2Задача 2Вопрос 3Задача 3Задача 4Вопрос 4Вопрос 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10Вопрос 11
§ 42:
Вопрос 1Задача 1Вопрос 2Задача 2Задача 3Вопрос 3Вопрос 4Вопрос 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10Вопрос 11
§ 40-41:
Вопрос 1Задача 1Вопрос 2Задача 2Вопрос 3Задача 3Задача 4Вопрос 4Вопрос 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10Вопрос 11Вопрос 12Вопрос 13Вопрос 14Вопрос 15
Глава V
Лабораторные опыты:
§ 34-38:
Вопрос 1Задача 1Задача 2Вопрос 2Задача 3Вопрос 3Вопрос 4Задача 4Вопрос 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10Вопрос 11Вопрос 12Вопрос 13Вопрос 14Вопрос 15
Глава III
Лабораторные работы:
Практические работы:
§15-18:
Задача 1Вопрос 1Вопрос 2Задача 2Вопрос 3Вопрос 4Вопрос 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10Вопрос 11Вопрос 12Вопрос 13Вопрос 14
§19-20:
задача 1вопрос 1задача 2вопрос 2вопрос 3задача 3вопрос 4вопрос 5вопрос 6вопрос 7вопрос 8вопрос 9
§21-23:
задача 1вопрос 1задача 2вопрос 2вопрос 3задача 3задача 4вопрос 4вопрос 5вопрос 6вопрос 7вопрос 8вопрос 9вопрос 10вопрос 11
Глава VIII
§ 45-47:
задача 1вопрос 1задача 2вопрос 2задача 3вопрос 3задача 4вопрос 4вопрос 5задача 5вопрос 6задача 6вопрос 7вопрос 8вопрос 9вопрос 10вопрос 11вопрос 12вопрос 13вопрос 14
Глава IV
Лабораторные работы:
§ 24-29:
задача 1вопрос 1задача 2вопрос 2задача 3вопрос 3вопрос 4задача 4задача 5вопрос 5вопрос 6вопрос 7вопрос 8вопрос 9вопрос 10вопрос 11вопрос 12вопрос 13вопрос 14вопрос 15вопрос 16вопрос 17вопрос 18вопрос 19вопрос 20вопрос 21вопрос 22вопрос 23
§ 30-33:
задача 1вопрос 1задача 2вопрос 2вопрос 3вопрос 4вопрос 5вопрос 6вопрос 7вопрос 8вопрос 9
Глава IX
Лабораторные опыты:
§ 48-54:
Задача 1Вопрос 1Вопрос 2Задача 2Вопрос 3Задача 3Вопрос 4Вопрос 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10Вопрос 11Вопрос 12Вопрос 13Вопрос 14Вопрос 15Вопрос 16Вопрос 17
§ 55-59:
Задача 1Вопрос 1Задача 2Вопрос 2Вопрос 3Задача 3Задача 4Вопрос 4Вопрос 5Задача 5Вопрос 6Вопрос 7Вопрос 8Вопрос 9Вопрос 10Вопрос 11Вопрос 12Вопрос 13Вопрос 14Вопрос 15
Опыт № 5. Распознавание сульфатов
Задание. Распознайте сульфат натрия с помощью качественной реакции.
Соблюдайте правила техники безопасности при работе с кислотами!
Оборудование. Штатив с пробирками.
Вещества. 5% -е растворы сульфата, хлорида и нитрата натрия, 10% -е растворы хлорида бария, серной, соляной и азотной кислот, порошок медного купороса, вода (в стакане).
1. В три пробирки налейте по 1 мл растворов сульфата натрия, хлорида натрия и нитрата натрия. В каждую из этих пробирок добавьте немного хлорида бария. Что вы наблюдаете?
Составьте полные и сокращенные ионные уравнения наблюдаемых реакций.
2. Докажите, что выданные вам голубые кристаллы содержат сульфат меди (II). Составьте уравнения реакций.
3. Налейте в три пробирки серную, азотную и соляную кислоты, добавьте в них раствор хлорида бария. Что вы наблюдаете? Напишите уравнения реакций.
Сделайте общий вывод, с помощью какого реактива можно распознать сульфат-ионы.
Наблюдается появление белого осадка в пробирке с сульфатом натрия. В других пробирках видимых изменений не наблюдается.
В пробирке с серной кислотой выпадет белый осадок. В других пробирках ничего не происходит.
Вывод: сульфат-ионы распознаются с помощью растворимых солей бария.
№5Лабораторные работы и опыты
Уникальные подробные решения с пояснениями Ответкина
Восьмой класс – непростой этап в обучении, переходное звено между средней и старшей школой. Домашние задания становятся трудоемкими, прибавляется количество уроков и факультативов, усложняется программа.
Нередко у восьмиклассников возникают сложности с освоением химии. В этой науке важна последовательность изложения материала, раскрывающего суть химических явлений и процессов. Если пропустить несколько занятий, отвлечься при объяснении новой темы – нужно срочно искать способы как восполнить пробелы в знаниях, чтобы не отстать по программе. В этой ситуации родители начинают подыскивать репетитора по химии. Но найти толкового и недорогого преподавателя сложно, кроме того дополнительные занятия подразумевают большие временные затраты.
Почему пособие с ГДЗ от Ответкина практичнее занятий с репетитором?
Способ получения
1. В результате взаимодействия разбавленной серной кислоты и гидроксида натрия образуется сульфат натрия и вода:
2. При температуре 450–800º C гидросульфат натрия реагирует с хлоридом натрия. В результате реакции образуется сульфат натрия и хлороводородная кислота:
NaHSO4+ NaCl = Na2SO4 + HCl
3. В состоянии кипения в результате реакции между твердым хлоридом натрия и концентрированной серной кислотой происходит образование сульфата натрия и газа хлороводорода:
4. Твердый сульфид натрия и кислород взаимодействуют при температуре выше 400º C с образованием сульфата натрия:
5. При взаимодействии концентрированного раствора пероксида водорода и сульфида натрия образуется сульфат натрия и вода:
Каким образом пособие по химии за 9 класс Рудзитис может помочь выпускнику и преподавателям
Сборник с ГДЗ предоставляет возможность:
- сократить время на подготовку без потери качества;
- совершить проверку своих знаний без посторонней помощи;
- повторить пройденный материал или восполнить пробелы в знаниях;
- подготовиться к итоговым выпускным испытаниям и увеличить вероятность получения нужного числа баллов.
Пособие по химии за 9 класс по химии (углубленный уровень) от Рудзитиса также может помочь учителям, занимающимся подготовкой детей к ЕГЭ индивидуально или на дополнительных занятиях. На основе приведенных задач учитель имеет шанс составить новые варианты упражнений и тестов для тренировки. Некоторые из таких заданий могут встретиться на экзамене.
Как определить сульфат натрия
Сульфат натрия относится к одному из четырех классов неорганических соединений – солям. Это бесцветное кристаллическое вещество, представляющее собой среднюю соль, состоящую из двух атомов натрия и кислотного остатка. В растворе соединение диссоциирует (распадается) на частицы – ионы натрия и сульфат-ионы, на каждый из которых проводится качественная реакция.

Вам понадобится
- – сульфат натрия;
- – нитрат или хлорид бария;
- – пробирки;
- – спиртовка или горелка;
- – проволока;
- – фильтровальная бумага;
- – щипцы или пинцет.
Инструкция
Для распознавания составных частей данной соли проведите две последовательные качественные реакции. Благодаря одной и них сможете определить натрий, вторая покажет наличие сульфат-ионов. Для определения натрия необходим нагревательный прибор, причем с открытым пламенем (электрический не сгодится). Возьмите проволочку, сделайте на одном конце петельку и прокалите ее на пламени. Это нужно для того, чтобы элементы, входящие в состав проволоки, не повлияли на результат и не исказили его. Затем опустите проволоку в раствор сульфата натрия, после чего внесите ее в пламя. Если появится ярко-желтое окрашивание пламени, то можете констатировать присутствие натрия.
Можно поступить несколько иначе. Возьмите фильтровальную бумагу, поместите ее в испытуемый раствор, вытащите и высушите. Повторите это несколько раз, чтобы концентрация ионов натрия увеличилась, что даст более интенсивную окраску пламени. С помощью тигельных щипцов или пинцета внесите небольшой кусочек бумаги в пламя. Изменение окраски будет также свидетельствовать о наличии натрия.
Для того чтобы определить сульфат-ион, необходимо провести на него качественную реакцию. Реагентом должно быть вещество, в состав которого обязательно входит ион бария. Для эксперимента возьмите, например, хлорид бария и прилейте в пробирку к исследуемому раствору. В емкости моментально произойдут изменения, так как выпадает осадок белого цвета сульфата бария. Это является показателем наличия сульфат-ионов. Аналогичное химическое явление будет наблюдаться, если для реакции возьмете и другую соль, содержащую ион бария. Главное условие, чтобы она была растворима в воде, что можно узнать по таблице растворимости солей, кислот и оснований.
Видео по теме
Обратите внимание
При проведении опытов обязательно соблюдайте правила техники безопасности, особенно при работе с нагревательными приборами.
Что поможет в освоении химии?
Девятиклассникам придется попотеть, чтобы добиться хороших результатов в учебе. Программа обучения становится в разы сложнее и объемнее. Кроме того, полным ходом идет подготовка к экзаменам. Не все школьники справляются с такими нагрузками. Многие, пытаясь сосредоточиться на нескольких задачах сразу, допускают повсюду промахи. Особенно сложно нагнать потом упущенные навыки по химии, так как эта наука весьма специфична. Поэтому лучше сразу предотвратить всякие недоразумения. Для этого достаточно воспользоваться справочником ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман (Просвещение, 2016 г.).
На девятом году обучения ученикам предстоит учить такие темы как:
- Окислительно-восстановительные реакции.
- Характеристика кислорода и серы.
- Сероводород. Сульфиды.
- Соли аммония.
- Фосфорная кислота и её соли.
- Химические свойства углерода. Адсорбция, и т.д.
Основные сложности возникают с составлением уравнений реакций, так как некоторые учащиеся не могут запомнить, что именно для этого надо. На уроках они списывают все с доски и не особо задумываются над тем, каким образом учитель приходит тем или иным выводам. Неудивительно, что дома подростки не могут повторить все продемонстрированные в классе схемы. Решебник позволит им разобраться во всех деталях и без всяких трудностей решать заданные номера.




























