Содержание учебника «Молекула. Физика. 7 класс. Перышкин»
Глава 1: Введение в молекулярную физику
1.1 Основные понятия и определения
1.2 Строение и свойства вещества
1.3 Движение молекул и его виды
Глава 2: Тепловое движение молекул
2.1 Кинетическая энергия и температура
2.2 Законы термодинамики и их применение
2.3 Изменение агрегатных состояний вещества
Глава 3: Диффузия и осмотическое давление
3.1 Диффузия и ее свойства
3.2 Осмотическое давление и его применение
Глава 4: Разделение смесей
4.1 Фильтрация, декантация и центрифугирование
4.2 Дистилляция и сублимация
4.3 Ионометрия и электродиализ
Глава 5: Молекулярная физика и электричество
5.1 Электростатика и законы Кулона
5.2 Электрический ток и его свойства
5.3 Электрическая цепь и основные ее элементы
Глава 6: Молекулярная физика и свет
6.1 Видимый свет и его свойства
6.2 Отражение и преломление света
6.3 Оптические явления и их объяснение
Глава 7: Молекулярная физика и магнетизм
7.1 Магнитные вещества и их свойства
7.2 Магнитное поле и его действие
7.3 Постоянные магниты и их использование
Приложения
1. Список основных формул и определений
2. Таблицы физических величин и констант
Структура молекулы
Молекула может состоять из одного вида атомов (например, кислородной молекулы O2) или из разных видов атомов (например, молекулы воды H2O, состоящей из атомов водорода и атомов кислорода). Атомы, входящие в молекулу, связаны между собой химическими связями.
Структура молекул может быть линейной, в которой атомы расположены последовательно друг за другом, или в виде различных геометрических форм, таких как углеродные кольца, октаэдры и т.д.
Молекула может быть аполярной, если все атомы в ней имеют одинаковую электроотрицательность и связи между атомами являются неполярными, или полярной, если атомы имеют различную электроотрицательность и образуют полярные связи.
Структура молекулы может быть представлена с помощью химической формулы, например, Н2О для воды или С6H12O6 для глюкозы. Эти формулы показывают состав молекулы и расположение атомов в ней.
Знание структуры молекулы позволяет предсказывать ее свойства и влияние на окружающую среду, а также проводить различные химические реакции с участием данной молекулы.
Строение молекулы
В мире существует огромное множество различных молекул с самыми разными свойствами. Самые простые молекулы состоят из одного атома. Пример такой одноатомной молекулы — благородные газы: гелий, неон, аргон, криптон, ксенон, радон. Большая часть молекул состоит из нескольких атомов, при этом атомы могут быть одинаковы, такими, к примеру, являются двухатомные молекулы кислорода, азота, многих других газов. Но чаще каждая молекула состоит из атомов различных видов (элементов).
Атомы внутри молекулы удерживаются электростатическими силами на определённых расстояниях, в зависимости от видов этих атомов. Более того, каждая молекула имеет свою пространственную структуру. Например, молекула углекислого газа состоит из трёх атомов, лежащих на одной прямой. А молекула воды — из трёх атомов, лежащих в вершинах равнобедренного треугольника, причём угол при вершине (атоме кислорода) составляет около 105 градусов.
Рис. 2. Структура молекулы воды
При сжатии молекулы возрастают силы отталкивания между атомами, при растяжении молекулы возрастают силы притяжения. Это обеспечивает стабильность молекул. Чтобы её разрушить, необходимо приложить энергию — химическую, термическую или электрическую.
Наиболее сложно устроены молекулы органических веществ. Эта сложность обуславливается тем, что атомы углерода могут соединяться друг с другом в длинные цепочки, одновременно присоединяя атомы других элементов. Самые большие молекулы — молекулы белков и основа генетики — молекула ДНК. В каждую такую молекулу могут входить сотни тысяч атомов. Один моль воды (моль содержит $6.022 \times 10^{23}$ молекул) весит 18 грамм. А 1 моль ДНК может весить свыше миллиона тонн.
Рис. 3. Структура молекулы ДНК.
Что мы узнали?
Молекула — это мельчайшая частица вещества, сохраняющая физические и химические свойства. Она состоит из одного и более атомов. Атомы образуют определённую пространственную структуру молекулы и удерживаются в таком виде электростатическими силами.
-
/5
Вопрос 1 из 5
Сложные и простые вещества
У сложных веществ молекулы состоят из атомов нескольких химических элементов. Например, молекула воды состоит из атомов кислорода и водорода, поэтому вода — сложное вещество.
У простых веществ молекулы состоят только из одного химического элемента. Например — кислород. Наглядное изображение приведено на рисунке 6.
Рисунок 6. Простые и сложные вещества
{"questions":[{"content":"Выберите правильное определение <b>молекул</b>.`choice-1`","widgets":{"choice-1":{"type":"choice","options":,"explanations":,"answer":}}},{"content":"Выберите правильное определение <b>атома</b>.`choice-10`","widgets":{"choice-10":{"type":"choice","options":,"explanations":,"answer":}}},{"content":"Составь схему строения вещества. Расположи понятия сверху вниз в порядке убывания.`sorter-28`","widgets":{"sorter-28":{"type":"sorter","items":}},"hints":},{"content":"Какие из ниже приведенных веществ являются сложными, а какие простыми?`grouper-60`","widgets":{"grouper-60":{"type":"grouper","labels":,"items":,]}},"hints":["У сложных веществ молекулы состоят из атомов нескольких химических элементов.<br />У простых веществ молекулы состоят только из одного химического элемента."]}]}
Размеры молекул
Каковы же размеры молекул? Если бы мы смогли уложить в один ряд 10 000 000 молекул воды, то получилась бы нить длиной в $2 \space мм$. А в $1 см^3$ воздуха содержится около $27 \cdot 10^{18}$ молекул.
Если представить, что маленькое отверстие пропускают по миллиону молекул в секунду, тогда указанное количество молекул пройдет только через 840 000 лет.
Еще интересный факт: если размер молекулы увеличить до размера точки в конце предложения в книге, то толщина человеческого волоса стала бы равна 40 м, а человек, стоя на поверхности Земли, упирался бы головою в Луну.
Современная наука позволяет нам увидеть эти малейшие составляющие нашего мира с помощью электронного микроскопа. На рисунке 1 представлены фотографии молекул, полученные с помощью электронного микроскопа, и их графическая интерпретация.
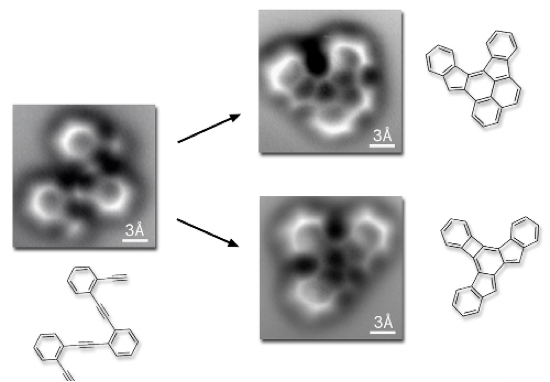
Рисунок 1. Фотографии молекул, полученные с помощью электронного микроскопа
Помните, что все тела, окружающие нас и похожие друг на друга, всегда будут различны. В природе вы не встретите ни двух одинаковых снежинок, ни людей, ни песчинок, ни животных, но молекулы одного и то же вещества всегда будут одинаковы.
Атомы и молекулы
Из курса физики 7 класса известно, что все тела состоят из молекул. Молекула является наименьшей частью вещества, определяющей его физические и химические свойства. Все огромное разнообразие веществ в природе — это следствие огромного числа различных видов молекул.
Но молекула не является наименьшей частью вещества. Химические превращения веществ (а значит, и молекул) доказывают, что молекулы имеют сложное строение. Большинство молекул могут быть разложены или синтезированы с помощью химических воздействий.
Мельчайшая частица вещества, которая не может быть разложена с помощью любых химических воздействий, называется атомом. Каждая молекула состоит из одного и более атомов. Все молекулы одного вещества имеют одинаковый состав и строение.
В отличие от многих миллионов видов молекул, число видов атомов в природе невелико. К середине XIX в. их было известно менее сотни. К настоящему времени в природе было найдено 94 элемента, и ещё 24 синтезированы искусственно.
Рис. 1. Атомы и молекулы.
Что такое молекула?
Молекулы могут быть одноатомными, то есть состоять только из одного вида атомов, например, молекула кислорода (O2) или молекула хлора (Cl2). Также молекулы могут быть сложными и состоять из разных атомов, например, молекула воды (H2O) состоит из атомов водорода и атома кислорода.
Молекулы имеют определенную форму и размеры, которые определяются взаимным расположением атомов в пространстве. Форма и размеры молекулы влияют на ее физические свойства, такие как температура кипения и плавления, плотность и растворимость.
Молекулы могут образовывать различные структуры — кристаллы и полимеры. Кристаллы представляют собой упорядоченный трехмерный решетчатый массив молекул, а полимеры — длинные цепочки молекул, связанных между собой.
Изучение молекул и их свойств является одним из основных направлений химии и физики. Понимание структуры и поведения молекул позволяет разрабатывать новые материалы и прогнозировать свойства вещества в различных условиях.
| Примеры молекул | Состав |
| Кислород (O2) | 2 атома кислорода |
| Вода (H2O) | 2 атома водорода, 1 атом кислорода |
| Аммиак (NH3) | 3 атома водорода, 1 атом азота |
| Углекислый газ (CO2) | 1 атом углерода, 2 атома кислорода |
Атомы
Будем ли мы считать молекулы самыми мельчайшими частицами? Например, если мы разделим молекулы воды, то свойства воды потеряются. Мы получим атомы двух химических элементов: 1 атом кислорода (O) и 2 атома водорода (H).
Термин «атом» переводится с греческого, как «неделимый», хотя современная наука уже опровергла данный факт, и вы узнаете об этом в следующих курсах физики.
Дадим определение.
Каждый атом — это химический элемент. Все химические элементы перечислены в таблице Менделеева (рисунок 2).
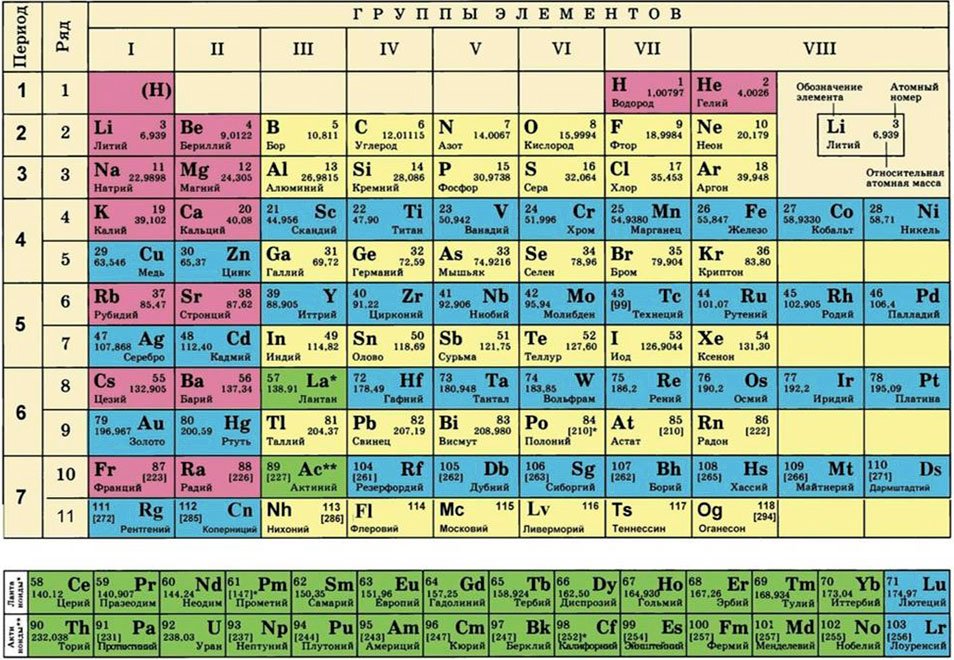
Рисунок 2. Периодическая таблица Менделеева
Мы можем сравнить атомы с буквами, при помощи которых собирается бесконечное количество слов — молекул. Таким образом, из атомов водорода и кислорода (взятые в разных количествах) мы получим молекулы разных веществ.
Например, если взять 2 атома водорода (H) и 1 атом кислорода(O), то получим молекулу воды $H_2 O$ (рисунок 3).
Рисунок 3. Молекула воды
А если взять 2 атома водорода (H) и 2 атома кислорода (O), то получим перекись водорода $H_2O_2$ (рисунок 4).
Рисунок 4. Молекула перекиси водорода
Итак, физические тела состоят из вещества, вещество состоит из молекул, а молекулы состоят из атомов (рисунок 5).
Рисунок 5. Схема строения вещества
Физика 7 класс Перышкин
В программе физики 7 класса учащиеся знакомятся с такими темами, как:
| Механическое движение | Электричество и магнетизм | Тепловые явления |
| Звук и свет | Оптика | Явления электрического тока |
Каждая тема в учебнике сопровождается объяснениями, иллюстрациями и практическими заданиями, которые помогают закрепить полученные знания и развить логическое мышление. Учебник Перышкина в 7 классе имеет структуру, удобную для усвоения материала, и строится на системной подаче информации.
Анализируя физику в 7 классе по учебнику Перышкина, можно отметить, что автор уделяет внимание не только теоретическим сведениям, но и практическим применениям физики в повседневной жизни
Это позволяет учащимся лучше осознать важность научных знаний и их применения в реальном мире
Изучение физики в 7 классе по учебнику Перышкина позволяет детям развить фундаментальные навыки научного мышления, укрепить понимание основных принципов и законов физики, а также подготовиться к дальнейшему изучению этой науки в более продвинутых классах.
Определение и свойства
Молекулы могут быть одноатомными или многоатомными. Одноатомные молекулы, такие как молекулы инертных газов, состоят из одного атома, например, молекула кислорода (O2). Многоатомные молекулы, такие как молекула воды (H2O) или молекула углекислого газа (CO2), состоят из двух или более атомов разных элементов.
Молекулы имеют определенные физические и химические свойства. Физические свойства молекул включают массу, размеры, форму, плотность, температуру вспышки и температуру кипения. Химические свойства молекул определяют их способность взаимодействовать с другими молекулами и средой, а также проводить химические реакции.
Молекулы могут существовать в различных фазах — газообразной, жидкой или твердой. В газообразной фазе молекулы располагаются на больших расстояниях друг от друга и движутся свободно. В жидкой фазе молекулы находятся близко друг к другу и имеют достаточную подвижность для образования течений. В твердой фазе молекулы располагаются в порядке и имеют малую подвижность.
- Молекулы имеют массу, которая измеряется в атомных единицах массы или килограммах.
- Молекулы могут иметь разные размеры и формы. Размеры молекул определяются расстояниями между атомами, а форма может быть линейной, угловатой или трехмерной.
- Плотность молекул определяет степень их упаковки в веществе. Молекулы с большей плотностью обычно имеют меньший объем.
- Температура вспышки молекулы — это минимальная температура, при которой молекула может загореться при воздействии открытого источника огня.
- Температура кипения молекулы — это температура, при которой молекула переходит из жидкого состояния в газообразное при нормальном атмосферном давлении.
Молекулы являются основными единицами всех химических и физических процессов, происходящих в веществах. Изучение свойств молекул позволяет понять механизмы химических реакций, фазовые переходы и множество других явлений в мире веществ.
Полный материал
Молекулы могут быть одноатомными, то есть состоять из одного атома, или многоатомными — состоять из двух или более атомов. Например, молекула кислорода (O_{2}) состоит из двух атомов кислорода, а молекула воды (H_{2})O состоит из двух атомов водорода и одного атома кислорода.
Молекулы обладают свойством колебаться и вращаться, что объясняет многие физические и химические свойства вещества. Также молекулы могут перемещаться в пространстве, образуя газообразное состояние вещества.
Изучение молекулы позволяет понять организацию вещества на микроуровне и объяснить его свойства и реакции. В физике и химии молекулы используются для объяснения явлений, таких как тепловое расширение, диффузия и электрохимические реакции.
Молекулы составляют основу всех веществ и играют важную роль в различных областях науки и техники. Изучение молекулы помогает улучшить процессы производства, разработать новые материалы и лекарственные препараты, а также понять природу и происхождение жизни на Земле.






























